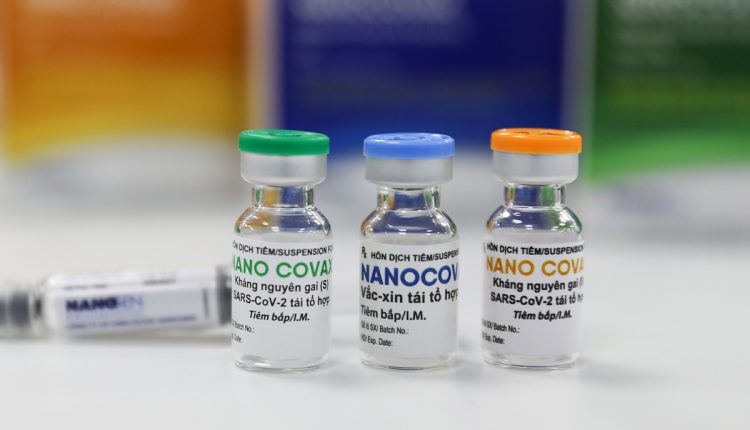
Bộ Y tế tiếp tục họp thẩm định vaccine Nano Covax
Ngày 15/8, Bộ Y tế dự kiến tiếp tục họp đánh giá kết quả lâm sàng pha 3a vaccine Nano Covax trước khi đề xuất về việc xem xét cấp phép khẩn.
Sáng 7/8, Hội đồng Đạo đức, Bộ Y tế, họp thẩm định kết quả thử nghiệm lâm sàng giai đoạn 1 và giữa kỳ giai đoạn 2 vaccine Nano Covax của Công ty Nanogen.
Bước đầu, các chuyên gia đánh giá vaccine an toàn, có tính sinh miễn dịch khá tốt, có hiệu quả bảo vệ với người tiêm, đặc biệt ở hàm lượng 25 mcg. Sau tiêm, 71% tình nguyện viên có phản ứng nhẹ bao gồm sốt, đau, sưng tại vị trí tiêm, một trường hợp phản ứng độ 2 nhưng không phải nhập viện.
Hội đồng Đạo đức cho rằng nhóm nghiên cứu cần tiếp tục theo dõi, đánh giá thêm về độ an toàn của vaccine, đồng thời cần đánh giá hiệu quả bảo vệ trên cỡ mẫu lớn hơn, khoảng 1.000 người.
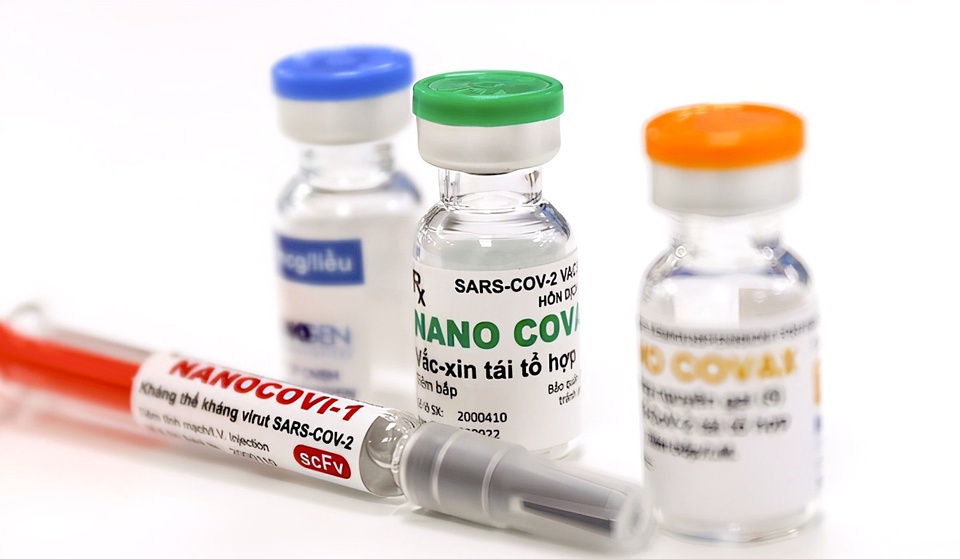
Trong báo cáo hỏa tốc của Nanogen gửi tối 5/8, thử nghiệm đánh giá tính sinh miễn dịch mới thực hiện trên 112 tình nguyện viên tiêm vaccine. Để có kết quả rõ hơn về độ an toàn, hiệu quả bảo vệ của vaccine, Hội đồng Đạo đức đề nghị Công ty Nanogen và nhóm nghiên cứu khẩn trương hoàn thiện báo cáo pha 3a, thử nghiệm trên 1.000 tình nguyện viên, gửi về Bộ Y tế ngay tuần tới.Vaccine Nano Covax sử dụng công nghệ protein tái tổ hợp.
Dựa trên báo cáo pha 3a, dự kiến ngày 15/8, Bộ Y tế tiếp tục tổ chức cuộc họp thẩm định. Nếu kết quả pha 3a tốt, Hội đồng Đạo đức sẽ có các đề xuất phù hợp với cơ quan có thẩm quyền để xem xét cấp phép khẩn cấp cho vaccine Nano Covax.
Vaccine Covid-19 của Công ty Nanogen sử dụng công nghệ protein tái tổ hợp, bắt đầu thử nghiệm lâm sàng giai đoạn 1 từ ngày 17/12/2020. Đến nay, Nano Covax là ứng viên vaccine ngừa Covid-19 nội tiềm năng nhất và đã bước vào thử nghiệm lâm sàng giai đoạn 3.
Trong đó giai đoạn 3a trên 1.000 tình nguyện viên đã hoàn tất tiêm mũi 2, giai đoạn 3b thử nghiệm trên 12.000 người đang tiêm nốt mũi 2, dự kiến hoàn tất trước ngày 15/8.
Đến nay, Nanogen đã 2 lần có văn bản xin đề nghị cấp phép khẩn cấp vaccine Nano Covax. Thời điểm gần nhất là tối 5/8, đơn vị này gửi báo cáo hoả tốc, trong đó gồm có công bố đánh giá của Viện Pasteur TP.HCM so sánh hiệu quả bảo vệ của vaccine dựa trên kết quả sinh miễn dịch với nhóm người mắc Covid-19 đã khỏi bệnh.
Kết quả ban đầu khá khả quan khi hiệu quả bảo vệ của vaccine Nano Covax cao gấp hơn 2 lần so với nhóm khỏi bệnh nhiễm chủng Vũ Hán, tương đương hiệu quả bảo vệ là 90% trong việc ngăn ngừa Covid-19 có triệu chứng. Một số tỉnh, thành phố đã có văn bản gửi Bộ Y tế xin được tham gia tiêm thử nghiệm vaccine Nano Covax trong bối cảnh nguồn cung vaccine còn hạn chế.
Trong cuộc họp sáng nay, Bộ Y tế đã giao Cục Khoa học công nghệ và Đào tạo có văn bản trả lời các tỉnh trên tinh thần đồng ý cho những địa phương này tham gia thử nghiệm nhưng phải đúng quy trình và đảm bảo an toàn. Sau Nano Covax, ứng viên vaccine Covid-19 thứ hai của Việt Nam là Covivac cũng sẽ bắt đầu thử nghiệm lâm sàng giai đoạn 2 trong tháng này.
Theo Zing